현재 국내에서 '코로나19' 관련해 임상시험이 진행 중인 치료제 및 백신은 총 20건으로 나타났다.
임상시험이 진행중인 '코로나 19 치료제'의 경우, 종근당 'CKD-314' 2상, 녹십자(GC녹십자) 'GC5131' 2상, 대웅제약 'DWRX2003' 1상 등이 포함됐다.
식품의약품안전처는 지난 8일 현재 국내에서 '코로나19' 관련해 임상시험이 진행 중인 치료제 및 백신은 총 20건이라고 밝혔다.
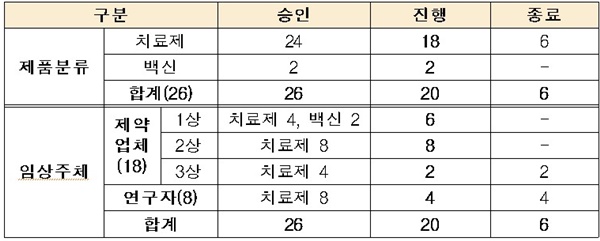
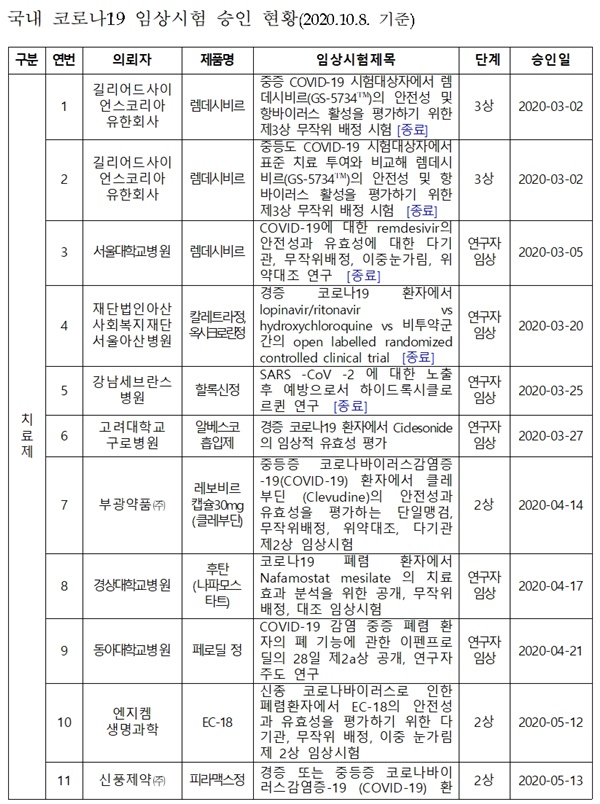
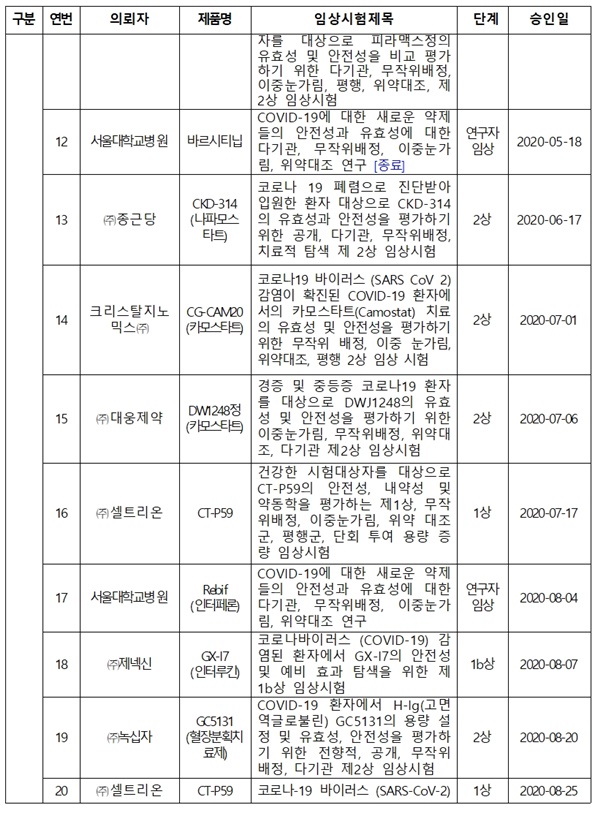
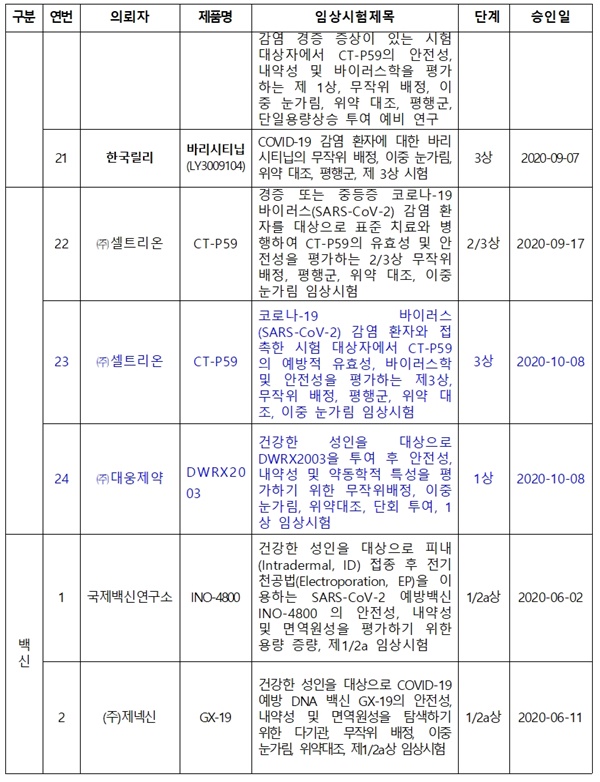
메디컬헤럴드가 최근 식약처가 발표한 '국내 코로나19 임상시험 승인 현황'<표 참조>을 확인한 결과, 현재 진행 중인 '코로나 19 치료제' 임상시험의 경우, 종근당 'CKD-314' 2상, 녹십자 'GC5131' 2상, 대웅제약 DWRX2003' 1상 등이 포함된 것으로 나타났다.
식약처 '국내 코로나19 임상시험 승인 현황'에 따르면, 국내 승인된 '코로나19 치료제 임상시험'의 경우, 고려대구로병원 알베스코흡입제 연구자 임상, 부광약품 '레보비르캡슐30mg'(클레부딘) 2상, 신풍제약 '피라맥스정' 2상, 서울대병원 '바르시티닙' 연구자 임상, 종근당 'CKD-314'(나파모스타트) 2상, 대웅제약 'DWJ1248정'(카모스타트) 2상, 녹십자 'GC5131'(혈장분획치료제) 2상, 대웅제약 'DWRX2003' 1상 등으로 나타났다.
국내 승인된 '코로나19 백신 임상시험'의 경우, 국제백신연구소 INO-4800 1/2a상, 제넥신 GX-19 1/2a상 등 2건이 해당된다.
식약처 '임상승인 현황'에 따르면, 종근당 'CKD-314'(나파모스타트)의 경우, 코로나19 폐렴으로 진단받아 입원한 환자 대상으로 CKD-314의 유효성과 안전성을 평가하기 위한 공개, 다기관, 무작위배정, 치료적 탐색 제 2상 임상시험 등 2상 임상시험이 승인됐다.
식약처는 국내 개발 코로나19 혈장분획치료제 'GC5131'(GC녹십자)에 대해 2상 임상시험을 지난 8월 20일 승인했다. 식약처에 따르면, 'GC5131'은 녹십자에서 코로나19 완치자의 혈장을 이용해 개발 중인 '고면역글로불린(Hyper-immune Globulin)' 성분 의약품으로, 코로나19 환자를 대상으로 안전성과 유효성을 평가하는 2상 임상시험을 진행하게 된다.
코로나19 완치자의 혈장에서 다양한 항체가 들어있는 면역 단백질을 분획해 만든 고면역글로불린(Hyperimmune globulin)은 오랜 기간 인체에 사용돼 온 제제이기 때문에 개발 과정이 간소화될 수 있다. 혈장치료제는 신종 감염병 발발 시 가장 빠르게 투약 가능한 의약품으로 분류된다.
식약처에 따르면, 대웅제약 'DWRX2003'의 경우, 현재 구충제로 사용되고 있는 성분(니클로사미드)으로 경구투여 시 체내 흡수율이 낮다는 단점이 있어, 대웅제약에서는 체내 흡수율을 높이기 위해 근육주사제로 개발됐다.
치료원리는 바이러스 등에 감염된 세포를 제거하는 자가포식(autophagy) 작용을 활성화해 바이러스 증식을 억제하는 방식이다. 'DWRX2003'는 인도에서 건강한 사람을 대상으로 임상시험을 진행 중에 있고, 필리핀에서는 코로나19 환자를 대상으로 한 임상시험이 승인되어 진행 중이다.